UNIDAD II
LA OXIDACIÓN Y REDUCCIÓN
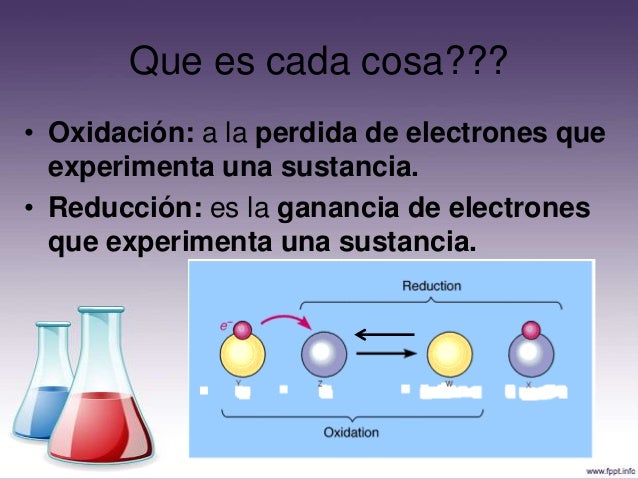
Un elemento se oxida cuando pierde electrones, la reduccion se da cuando el elemento gana electrones por lo tanto se hace negativo.
OXIDACION
La oxidacion ocurre cuando una especie quimica oierde electrones y al mismo tiempo aunmenta su numero de oxidacion. por ejemplo, el sodio metalico ( con numero de oxidacion de cero) se puede comvertir en iones solido (con carga de 1+) por la perdida de dos electrones segun el esquema siguiente
Na(0) ---> Na (1+) + 1e-
En resumen
oxidacion= pierde su numero de electrones y aumenta su numero de oxidacion
REDUCCION
La reduccion ocurre cuando cuando una especie quimica gana electrones y simuladamente disminuye su numero de oxidacion. por ejemplo el cloro atomico (con numero de oxidacion de cero )
se combierte en el ion cloruro (como numero de oxidasion y de carga 1-) por ganancia de un electron
1e- + Cl (0) ----> Cl (1-)
En resumen
reduccion= gana electrones y disminuye su numero de oxidacion.

ESTEQUIOMETRIA
Es la parte de la quimica que estudia las cantidades de la matearia (masa o volumen)
encontrados en una reaccion quimica.
para realizar estas determinaciones es nesesario tomar en cuenta los siguientes conseptos
||1|| MASA:
se refiere a los gramos o kilogramos de reactivs en las reacciones quimicas
en si que es la masa pues esta es la medida que que indica la cantidad de matearia que tiene un cuerpo. un cuerpo corresponde a una porcion de materia que puede encontrase en estado solido, liquido o gaseoso el cual debe estar formado por materiales de igual o diferente naturaleza.

||2|| VOLUMEN
Son los mililitros o litros que se utiliza como reactivos o productos
el volumen es el que corresponde a la medida del espacio que ocupa un cuerpo. la unidad para medir el volumen en metros cubicos, sin embargo generalmente se utilizan litros para ello.

||3||PESO MOLECULAR
Se obtiene a sumar los pesos atomicos de los elementos en un compuesto
el peso es la fuerza de la tierra con que la atrae a un cuerpo, el termino también se utiliza para la magnitud de dicha fuerza. lo correcto es hablar que el peso molecular sobre estos dos componentes

||4||MOL
es la unida que se utilaza unicamente en area quimica y reacciona a la masa y el peso molecular de un compuesto de elemento
el mol es una unidad que se mide la cantidad de sustancia, una de las 7 magnitudes físicas fundamentales, el numero de unidades elementarias son los iones, átomos, moléculas, electrones, radicales u otras partículas o grupos específicos de esta, el mol equivale a lo siguiente definición, una constante que no depende del material ni del tipo de partícula considerado.
DETERMINACIÓN DE NUMERO DE PESO MOLECULAR
este termino se utiliza para indicar la relación que existe entre la masa y el peso molecular de un elemento o compuesto. es una unidad básica que se utiliza se utiliza únicamente en el área química
para calcular los moles de una sustancia se requiere conocer:
||1||-la masa atómica de cada uno de los elementos que constituye la sustancia
||2||-determinar la masa molecular
para determinar los moles se debe utilizarla la siguiente expresión matemática
N=NUMERO DE MOLES
a= GRS DE SUSTANCIA
||1|| determinar el de átomos y moléculas que tiene la sustancia
||2|| las masas atómicas, dato que se obtiene en la tabla periódica
||3||sumar las masas atómicas de cada uno de los elementos que constituye la molécula



 DETERMINACIÓN DE MASA
DETERMINACIÓN DE MASA
densidades de objetos de interés usando distintos tipos de balanzas y métodos experimentales. ... Inferencia de la composición de la Tierra a partir del análisis de la densidad de la misma. Introducción. La densidad, ρ, de un cuerpo se define como la masa por unidad de volumen.Para poder determinar los valores de la masa necesario despejar la formula con la que se calcula el numero de moles para que quede de la siguiente manera.
n= p m=(n) (pm)
pm
DETERMINACIÓN DE MASA EN REACCIONES QUÍMICAS
Para poder determinar una cantidad de masa en una reacción química es necesario seguir el procedimiento que se indica.


Un elemento se oxida cuando pierde electrones, la reduccion se da cuando el elemento gana electrones por lo tanto se hace negativo.
OXIDACION
La oxidacion ocurre cuando una especie quimica oierde electrones y al mismo tiempo aunmenta su numero de oxidacion. por ejemplo, el sodio metalico ( con numero de oxidacion de cero) se puede comvertir en iones solido (con carga de 1+) por la perdida de dos electrones segun el esquema siguiente
Na(0) ---> Na (1+) + 1e-
En resumen
oxidacion= pierde su numero de electrones y aumenta su numero de oxidacion
REDUCCION
La reduccion ocurre cuando cuando una especie quimica gana electrones y simuladamente disminuye su numero de oxidacion. por ejemplo el cloro atomico (con numero de oxidacion de cero )
se combierte en el ion cloruro (como numero de oxidasion y de carga 1-) por ganancia de un electron
1e- + Cl (0) ----> Cl (1-)
En resumen
reduccion= gana electrones y disminuye su numero de oxidacion.

ESTEQUIOMETRIA
Es la parte de la quimica que estudia las cantidades de la matearia (masa o volumen)
encontrados en una reaccion quimica.
para realizar estas determinaciones es nesesario tomar en cuenta los siguientes conseptos
||1|| MASA:
se refiere a los gramos o kilogramos de reactivs en las reacciones quimicas
en si que es la masa pues esta es la medida que que indica la cantidad de matearia que tiene un cuerpo. un cuerpo corresponde a una porcion de materia que puede encontrase en estado solido, liquido o gaseoso el cual debe estar formado por materiales de igual o diferente naturaleza.

||2|| VOLUMEN
Son los mililitros o litros que se utiliza como reactivos o productos
el volumen es el que corresponde a la medida del espacio que ocupa un cuerpo. la unidad para medir el volumen en metros cubicos, sin embargo generalmente se utilizan litros para ello.

||3||PESO MOLECULAR
Se obtiene a sumar los pesos atomicos de los elementos en un compuesto
el peso es la fuerza de la tierra con que la atrae a un cuerpo, el termino también se utiliza para la magnitud de dicha fuerza. lo correcto es hablar que el peso molecular sobre estos dos componentes

||4||MOL
es la unida que se utilaza unicamente en area quimica y reacciona a la masa y el peso molecular de un compuesto de elemento
el mol es una unidad que se mide la cantidad de sustancia, una de las 7 magnitudes físicas fundamentales, el numero de unidades elementarias son los iones, átomos, moléculas, electrones, radicales u otras partículas o grupos específicos de esta, el mol equivale a lo siguiente definición, una constante que no depende del material ni del tipo de partícula considerado.


DETERMINACIÓN DE NUMERO DE PESO MOLECULAR
este termino se utiliza para indicar la relación que existe entre la masa y el peso molecular de un elemento o compuesto. es una unidad básica que se utiliza se utiliza únicamente en el área química
para calcular los moles de una sustancia se requiere conocer:
||1||-la masa atómica de cada uno de los elementos que constituye la sustancia
||2||-determinar la masa molecular
para determinar los moles se debe utilizarla la siguiente expresión matemática
N = a
MM
DONDE N=NUMERO DE MOLES
a= GRS DE SUSTANCIA
M= MASA MOLECULAR
PARA CALCULAR LA MASA MOLECULAR SE REQUIERE
||2|| las masas atómicas, dato que se obtiene en la tabla periódica
||3||sumar las masas atómicas de cada uno de los elementos que constituye la molécula




densidades de objetos de interés usando distintos tipos de balanzas y métodos experimentales. ... Inferencia de la composición de la Tierra a partir del análisis de la densidad de la misma. Introducción. La densidad, ρ, de un cuerpo se define como la masa por unidad de volumen.Para poder determinar los valores de la masa necesario despejar la formula con la que se calcula el numero de moles para que quede de la siguiente manera.
n= p m=(n) (pm)
pm
DETERMINACIÓN DE MASA EN REACCIONES QUÍMICAS
Para poder determinar una cantidad de masa en una reacción química es necesario seguir el procedimiento que se indica.
- determinar que la reacción química este valenciana.
- hacer planteamiento del problema.
- determinar un primer valor de un numero de moles a que se les da nombre de cada dato de base.
- se obtiene el resto de valores de un numero de moles multiplicando el dato base por el coeficiente cada compuesto tiene en la reacción.
- se obtiene los valores de masa multiplicando el numero de moles para el peso molecular correspondiente
- se puede comprobar procedimiento sumando la masa de los reactivos que debe ser igual a la masa de los productos


Buen blog, muy lleno de información para alumnos con problemas en Quimica.
ResponderEliminarEl Blog esta muy extenso y ademas bien explicado.
ResponderEliminar